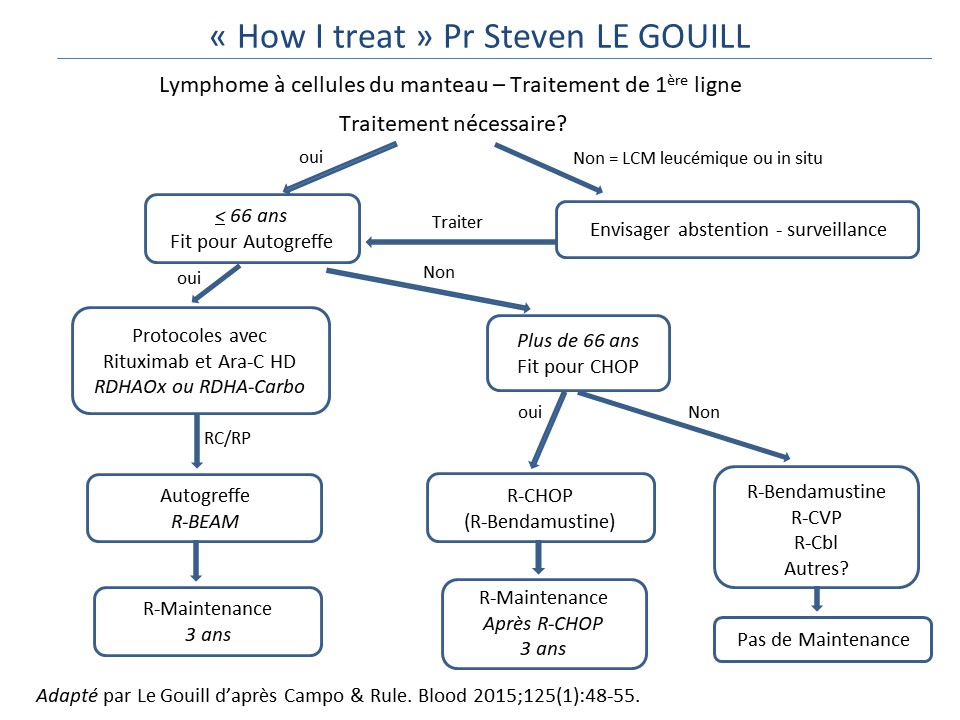
Lymphome à cellules du manteau – Traitement de 1ère ligne
Stade I ou stade II avec atteinte contigüe non volumineuse
ISRT (involved site RT)
ou immunochimiothérapie (schémas moins agressifs) +/- ISRT
Stade II avec atteinte non contigüe non volumineuse
immunochimiothérapie (schémas moins agressifs)
Ou abstention surveillance dans des situations très sélectionnées (MIPI faible, cytogénétique normale, absence d’altération de TP53)
Stade II avec atteinte volumineuse ou non contigüe, stades III et IV
TP53 classique type non muté
Patients éligibles pour traitement d’induction agressif
Essai clinique ou immunochimiothérapie traitements d’induction agressifs
CR Entretien BTKi + rituximab
ou intensification thérapeutique – autogreffe cellules souches et entretien BTKi + rituximab
PR Immunochimiothérapie pour obtenir RC
ou BTKi suivi d’entretien jusqu’à progression
Stable ou progression : traitement des formes réfractaires/rechutes
Patients non éligibles pour traitement d’induction agressif
Essai clinique ou immunochimiothérapie traitements d’induction moins agressifs
- CR envisager entretien rituximab
- PR traitement de 2ème ligne pour obtenir CR suivi d’entretien rituximab
- Stable ou progression : traitement formes réfractaires rechutes
Formes indolentes
Biomarqueurs SOX11, IGHV muté
Présentation clinique leucémique non ganglionnaire de type LLC, avec splénomégalie, atteinte digestive ou sang/moelle seulement, faible masse tumorale, fraction de prolifération Ki-67 < 10%
Asymptomatique sans autre indication thérapeutique : surveillance
Symptomatique ou autre indication thérapeutique : évaluer en cas de suspicion clinique concernant une évolution / nouvelle biopsie et séquençage du gène TP53
Traitements d’induction
Traitements d’induction agressifs
LyMA RDHA + platine (carboplatine ou platine ou oxaliplatine) x 4 + R-CHOP si non CR-PET
NORDIC : maxi R-CHOP + aracytine HD
R-bendamustine suivi de rituximab-aracytine HD
TRIANGLE : alternance R-CHOP + BTKi / R-DHAP
Autres traitements : Hyper CYVAD + rituximab
Traitements d’induction moins agressifs
Bendamustine-rituximab
VR-CAP (bortezomib, rituximab, cyclophosphamide, doxorubicine, prednisone)
R-CHOP + entretien rituximab
Lenalidomide rituximab
Autres traitements R-BAC500 (rituximab, bendamustine, cytarabine)
Traitement d’entretien
Traitements d’entretien après HDT-ASCT ou traitements d’induction agressifs
BTKi x 2 ans + Rituximab / 8 semaines x 3 ans
Traitements d’entretien après traitements d’induction moins agressifs et réponse complète
Envisager entretien Rituximab / 8 semaines x 2-3 ans après R-CHOP ou R-bendamustine
ESMO GUIDELINES 2017
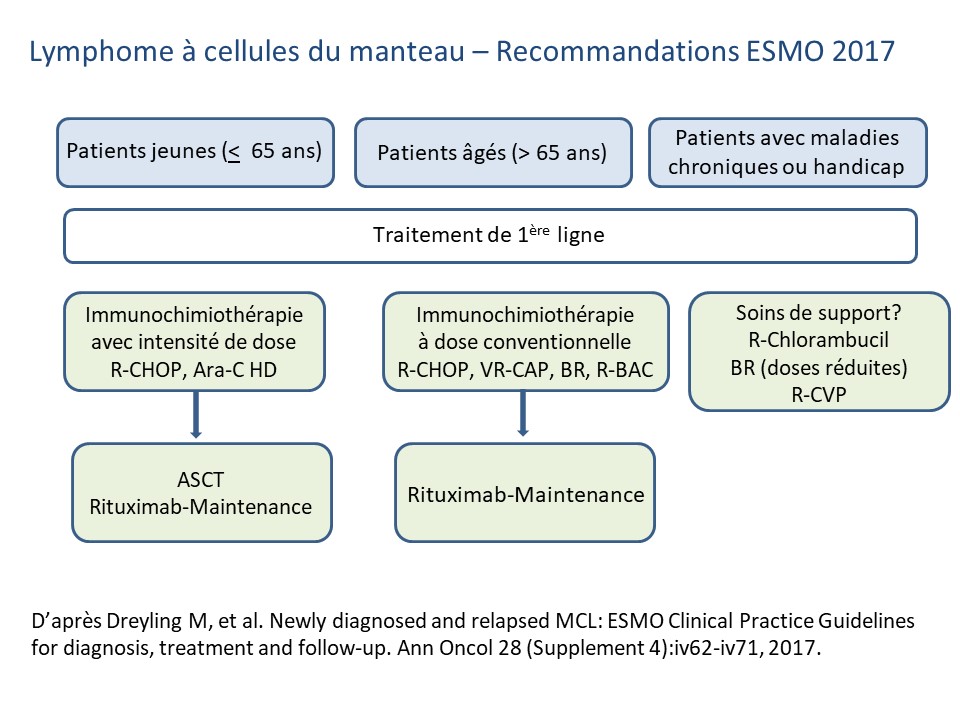
Stade I-II non bulky
Immunochimiothérapie (courte) + IFRT 30-36 Gy
Stade I-II avec atteinte volumineuse ou facteurs de risque
Immunochimiothérapie +/- RT selon localisation et effets indésirables attendus.
Stade III-IV patients < 65 ans
Immunochimiothérapie (avec Aracytine HD) + ASCT + entretien Rituximab
Patients > ou = 65 ans
Immunochimiothérapie : R-CHOP, R-Bendamustine, R-BAC (Bendamustine Cytarabine) + entretien Rituximab
Patients avec comorbidités
R-Chlorambucil, R-Bendamustine doses réduites
Cet algorithme de traitement reprend les grandes lignes de celui publié par Elias Campo et Simon Rule dans Blood, en 2015. Depuis le recours au traitement d’entretien par rituximab a été élargi aux patients autogreffés pour une durée fixe de 3 ans. A noter que chez les patients plus âgés, le bénéfice du rituximab en maintenance est établi seulement après R-CHOP. Le nombre de cycle de R-CHOP peut être discuté, mais la référence à ce jour est de 8 cycles tous les 21 jours. Cette stratégie de traitement se base sur des études de phase 3. On s’attend cependant à ce que l’arrivée des thérapies dites ciblées (et en premier lieu l’Ibrutinib) vienne quelque peu bousculer rapidement cette stratégie.
Prof. Steven LE GOUILL, service d’hématologie clinique, CHU de Nantes
Traitement des patients éligibles pour une intensification thérapeutique avec autogreffe : induction chimio-immunothérapie avec Ara-C Haute Dose et rituximab + Chimiothérapie intensive avec autogreffe de CSP + entretien rituximab 3 ans
Valeur prédictive de l’évaluation de la maladie résiduelle (MRD) après induction et dans le suivi
Questions en débat
Durée du traitement d’entretien par rituximab chez le sujet âgé
Place de l’AraC en induction chez le sujet âgé et d’une maintenance renforcée par lenalidomide –Rituximab.
Place des traitements sans chimiothérapie (« chemo-free ») en première ligne et en rechute (par ex : Obinutuzumab + Vénétoclax + Ibrutinib)
Après traitement Bendamustine et rituximab, le bénéfice d’un entretien par rituximab n’a pas été démontré dans les essais cliniques prospectifs
Perspectives
A évaluer dans les essais cliniques
Définir de nouveaux index pronostic comportant des marqueurs biologiques
Traitement guidé par TEP et MRD
Traitement des patients jeunes sans HDT-ASCT
Traitement des LCM à haut risque
Place des thérapies ciblées en 1ère ligne, alternative possible en cas de contre-indication à la chimiothérapie (inhibiteur de Bcl2 vénétoclax, inhibiteurs de BTK)
Traitements innovants : cellules CAR-T, ATU en rechute (2 lignes de traitement préalables, dont inhibiteur de BTK).
Référence
Cohen JB, Zain JM, and Kahl BS. Current approach to mantle cell lymphoma: Diagnosis, prognosis and therapies. ASCO Educational Book 2017:512-525.
Dreyling M, Campo E, Hermine O, et al. Newly diagnosed and relapsed mantle cell lymphoma : ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Ann Oncol 28 (Supplement 4):iv62-iv71, 2017.
Elias Campo and Simon Rule. Mantle cell lymphoma: evolving management strategies. Blood 2015;125(1):48-55.
Hoster E, Dreyling M, Klapper W, et al. A new prognostic index (MIPI) for patients with advanced-stage mantle-cell lymphoma. Blood 2008;111:558-565.
Ladha, A, Zhao J, Epner EM and Pu JJ. Mantle cell lymphoma and its management: where are we now? Exp Hematol Oncol 8, 2 (2019). https://doi.org/10.1186/s40164-019-0126-0
Le Gouill S, Beldi-Ferchiou A, Alcantara M, et al. Molecular response after obinutuzumab plus high-dose cytarabine induction for transplant-eligible patients with untreated mantle-cell lymphoma (LyMa-101): a phase 2 trial of the LYSA group. Lancet Hematol 2020; (published online Sept 21.)
https://doi.org/10.1016/ S2352-3026(20)30291-X
Pott C, Hoster E, Delfau-Larue MH, et al. Molecular remission is an independent predictor of clinical outcome in patients with mantle cell lymphoma after combined immunochemotherapy: a European MCL intergroup study. Blood 2010;115:3215-2323.
Witzens-Harig M, Hess G, Atta J, et al. Current treatment of mantle cell lymphoma: results of a national survey and consensus meeting. Ann Hematol (2012) 91:1765-1772.